濃さとは
更新日:

食塩水の問題は、上位校の入試に良く出題されるタイプの問題だ。
濃度を扱う問題は、高校入試や大学入試でも出題されるし、かなり難易度が高い。
10%の食塩水50グラムに溶けている食塩の量は?みたいな簡単な問題もある。
30%の濃度の食塩水を100グラム作るには?みたいな(比較的)簡単な問題もある。
しかし難関中学の入試では、濃さの異なる食塩水が数種類出てきて、それを操作する事が多い。
たとえば濃さの異なる食塩水を混ぜたり、二つに分けて片方に水を加えたり、水分を蒸発させたり。
こういう様々な「操作」によって、最初の食塩水の濃度を求めたり、加えた水の量や蒸発した水分量を求めたりする。
食塩水の問題は、いくらでも難しい問題が作れるので、中位校以上の入試では必ずと言って出題される。
ところがこういう食塩水の濃度問題は、小学生にはかなり難しい。
というのも濃度の定義が、ピンとこないかららしい。
濃さの問題を解くには?
濃さは、溶質÷溶液で表される割合のことだ。
溶質(ようしつ)とは、溶けている物質のことで、食塩水だと食塩が溶質だ。
溶液とは、溶質が溶けている液体のことで、食塩水全体のことを指す。
濃さはパーセントで表すことが多い。
具体的には、果汁50%のジュース1Lだと、1L中の500mLが果汁で、残りの500mLが水になる。
果汁30%のジュース1Lだと、300mLが果汁で、残りの700mLが水になる。
これだけなら、そんなに複雑な計算にはならない。
ところがちょっと操作が加わると、一気に難易度が上がってしまう。
濃さと溶液量(全体の重さ)、溶質量(食塩の重さ)の関係がちゃんと理解できていないと、まず解けない。
濃さの問題を解くには?
濃さの問題を解くには、まず「食塩水の基本図」を描く必要がある。
食塩水の図というのは、食塩水と濃度と食塩量を縦に並べた図のことだ。
具体的には、次のような図になる。
食塩水の基本図の一例
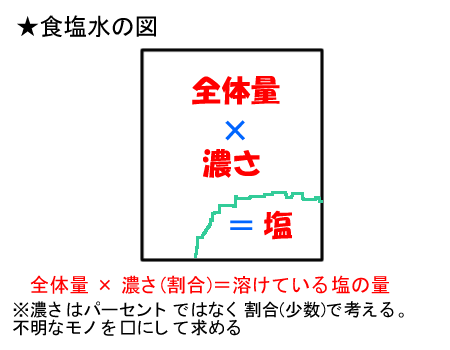
食塩水の量と濃さの位置は入れ替えても良い。
一番上に濃度、次に全体量という風に描くヒトも多い。
上の二つは掛け算するので、どちらが上でも構わないが、自分でどちらを上に描くかは、決めておかねばならない。
というのも、この図を食塩水の数だけ描いて足したり引いたりするからだ。
6年生の夏以降の家庭学習ミニ模試に
楽天ブックス(広告)














